Juhtivusmõõtmise tööstuselektroodide seeria on spetsiaalselt ette nähtud puhta vee, ülipuhta vee, veetöötlusseadmete jms juhtivuse mõõtmiseks. See sobib eriti hästi juhtivuse mõõtmiseks soojuselektrijaamades ja veetöötlustööstuses. Seda iseloomustab kahesilindriline struktuur ja titaanisulamist materjal, mis saab looduslikult oksüdeeruda keemilise passiivsuse moodustamiseks. Selle infiltratsioonivastane juhtiv pind on vastupidav igat tüüpi vedelikele, välja arvatud fluoriidhape. Temperatuuri kompenseerivad komponendid on: NTC2.252K, 2K, 10K, 20K, 30K, ptl00, ptl000 jne, mille määrab kasutaja. K=10.0 või K=30 elektrood kasutab suurt plaatina struktuuri pinda, mis on vastupidav tugevatele hapetele ja leeliselistele ning millel on tugev reostusvastane võime; seda kasutatakse peamiselt juhtivuse väärtuse reaalajas mõõtmiseks spetsiaalsetes tööstusharudes, nagu reoveepuhastus ja merevee puhastamine.
| Elektroodi konstant | 0,1 | 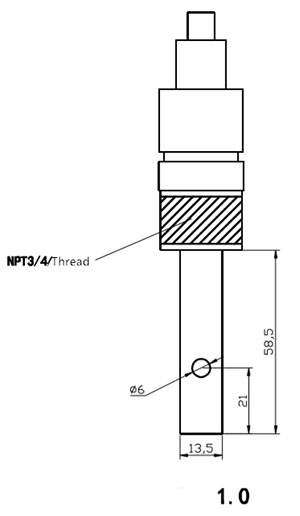 |
| Survetugevus | 0,6 MPa | |
| Mõõtevahemik | 0–200 μS/cm | |
| Ühendus | 1/2 või 3/4 keermega paigaldus | |
| Materjal | 316L roostevaba teras | |
| Taotlus | Veetöötlustööstus |
Juhtivuson vee võime mõõt elektrivoolu läbi lasta. See võime on otseselt seotud ioonide kontsentratsiooniga vees.
1. Need juhtivad ioonid pärinevad lahustunud sooladest ja anorgaanilistest materjalidest, nagu leelised, kloriidid, sulfiidid ja karbonaatühendid
2. Ioonideks lahustuvaid ühendeid nimetatakse ka elektrolüütideks 40. Mida rohkem ioone on vees, seda suurem on selle juhtivus. Samamoodi, mida vähem ioone vees on, seda vähem see juhtiv on. Destilleeritud ehk deioniseeritud vesi võib oma väga madala (kui mitte tühise) juhtivuse tõttu toimida isolaatorina. Mereveel on seevastu väga kõrge juhtivus.
Ioonid juhivad elektrit oma positiivsete ja negatiivsete laengute tõttu
Kui elektrolüüdid vees lahustuvad, lagunevad nad positiivselt laetud (katioonid) ja negatiivselt laetud (anioonid) osakesteks. Lahustunud ainete lagunemisel vees jäävad positiivse ja negatiivse laengu kontsentratsioonid võrdseks. See tähendab, et kuigi vee juhtivus ioonide lisamisega suureneb, jääb see elektriliselt neutraalseks.²






















